锥虫是一种血鞭毛原虫(hemoflagellate protozoa),寄生于鱼类、两栖类、爬虫类、鸟类、哺乳类以及人的血液或组织细胞内。寄生于人的锥虫依其感染途径可分为两大类,即通过唾液传播的涎源性锥虫与通过粪便传播的粪源性锥虫。
一、冈比亚锥虫与罗得西亚锥虫
冈比亚锥虫(Trypanosoma gambiense Dutton,1902)与罗得西亚锥虫(T.rhodesiense Stephens & Fantham,1910)同属于人体涎源性锥虫,是非洲锥虫病(african trypanosomiasis)或称睡眠病(sleeping sickness)的病原体。冈比亚锥虫分布于西非和中非靠近河边的环境中,而罗得西亚锥虫分布于东非的大草原上。两种锥虫在形态、生活史、致病及临床表现有共同特征。
形态与生活史
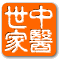
两种锥虫在人体内寄生,皆为锥鞭毛体(trypomastigote),具多形性(pleomorphism)的特点,可分为细长型、中间型和粗短型(图11-4)。在用姬氏液或瑞氏液染色的血涂片中,虫体胞质呈淡蓝色,核居中,呈红色或红紫色。动基体为深红色,点状。波动膜为淡蓝色。细胞质内有深蓝色的异染质(volutin)颗粒。细长型长20~40µm,游离鞭毛可长达6µm,动基体位于虫体后部近末端。粗短型长15~25µm,宽3.5µm,游离鞭毛短于1µm,或者鞭毛不游离,动基体位于虫体近后端。动基体为腊肠型,含DNA,一端常生出细而长的线粒体。鞭毛起自基体,伸出虫体后,与虫体表膜相连。当鞭毛运动时,表膜伸展,即成波动膜。
这两种锥虫的锥鞭毛体,在病程的早期存在血液、淋巴液内,晚期可侵入脑脊液。在三型锥鞭毛体中,仅粗短型对舌蝇具有感染性。雄或雌舌蝇吸入含锥鞭毛体的血液,在中肠内,粗短型进行繁殖,并转变为细长的锥鞭毛体,以二分裂法增殖。约在感染10天后,锥鞭毛体从中肠经前胃到达下咽,然后进入唾腺。在唾腺内,锥鞭毛体附着于细胞上,并转变为上鞭毛体(epimastigotes)。要过增殖最后转变为循环后期锥鞭毛体(metacyclic trypomastigotes),其外形短粗,大小约15×2.5µm,无鞭毛,对人具感染性。当这种舌蝇刺吸入血时,循环后期锥鞭毛体随涎液进入皮下组织,转变为细长型,繁殖后进入血液(图11-4)。

图11-4 锥虫生活史
致病
两种锥虫侵入人体以后的基本过程包括:锥虫在局部增殖所引起的局部初发反应期,锥虫在体内散播的血淋巴期以及侵入中枢神经系统的脑膜脑炎期。
初发反应期 锥虫在侵入的局部增殖,引起由淋巴细胞、组织细胞及少数嗜酸性粒细胞和巨噬细胞组成的细胞浸润,局部红肿,称锥虫下疳(trypanosomal chancre)。锥虫下疳约在感染后第6天出现,初为结节,以后肿胀,形成硬结,有痛感,约3周后消退。
血淋巴期 锥虫进入血液和组织间淋巴液后,出现广泛淋巴结肿大,淋巴结中的淋巴细胞、浆细胞和巨噬细胞增生。感染后约5~12天,血中出现锥虫。由于保护性抗体的出现及虫体抗原变异,血中锥虫数目出现交替上升与下降现象,间隔时间约为2~10天,虫血症高峰持续2~3天,伴有发热、头痛、关节痛、肢体痛等症状。发热持续数天,可自行下降进入无热期,隔几天后再次上升。淋巴结普遍肿大,尤以颈后部、颌下、腹股沟淋巴结为显著。颈部后三角部淋巴结肿大(Winterbottom氏征)是冈比亚锥虫病的特征。还可出现深部感觉过敏(Kerandel氏征),脾充血、肿大。可发生心肌炎、心外膜炎及心包积液。
脑膜脑炎期 锥虫侵入中枢神经系统可在发病后几个月或数年才出现。锥虫入侵后发生弥漫性软脑膜炎,脑皮质充血和水肿,神经元变性,胶质细胞增生。主要表现为个性改变、无欲状态,以后出现异常反射,深部感觉过敏、共济失调、震颤、痉挛、嗜睡,最后昏睡。
两种锥虫病的病程有所不同,冈比亚锥虫病呈慢性过程,病程数月至数年。罗得西亚锥虫病呈急性过程,病程为3~9个月。有些病人在中枢神经系统未受侵犯以前,即死亡。
诊断
涂片检查 取患者血液涂片染色镜检。当血中虫数多时,锥鞭毛体以细长型为主,血中虫数因宿主免疫反应而下降时,则以粗短型居多。淋巴液、脑脊液、骨髓穿刺液、淋巴结穿刺物也可涂片检查。
血清学诊断方法 常用酶联免疫吸附试验(ELISA)、间接荧光抗体试验、间接血凝试验。
分子生物学方法 近年来将PCR及DNA探针技术应用于锥虫病诊断,特异性、敏感性均较高。
此外,动物接种也是一种有用的检查方法。
流行和防治
冈比亚锥虫病的主要传染源为病人及感染者。牛、猪、山羊、绵羊、犬等动物可能是储存宿主。主要传播媒介为须舌蝇(Glossina palpalis)、G.tachinoides和G.fuscipes。这类舌蝇在沿河边或森林的稠密植物地带孳生。
罗得西亚锥虫病的传染源为动物及人。主要传播媒介为刺舌蝇(G.morsitans)、淡足舌蝇(G.pallidipes)种团及G.swynnertoni。这类舌蝇孳生在东非热带草原和湖岸的矮林地带及植丛地带,嗜吸动物血,在动物中传播锥虫,人因进入这种地区而感染。
防治 锥虫病的主要措施包括发现、治疗病人和消灭舌蝇。治疗药物苏拉明(suramine)对两种锥虫早期均有效。如锥虫已侵犯中枢神经系统,须用有机砷剂。改变孳生环境,如清除灌木林,喷洒杀虫剂能有效消灭舌蝇。
二、枯氏锥虫
枯氏锥虫(Trypanosoma cruzi,Chagas,1909)属人体粪源性锥虫,是枯氏锥虫病即夏格氏病(Chaga's disease)的病原体。主要分布于南美和中美,故又称美洲锥虫病。
形态
枯氏锥虫在它的生活史中,因寄生环境不同,有三种不同形体:无鞭毛体、上鞭毛体和锥鞭毛体。
无鞭毛体(amastigote)存在于细胞内,圆形或椭圆形,大小为2.4~6.5µm,具核和动基体,无鞭毛或有很短鞭毛。
上鞭毛体(epimastigote)存在于锥蝽的消化道内,纺锤形,长约20~40µm,动基体在核的前方,游离鞭毛自核的前方发出。
锥鞭毛体存在于血液或锥蝽的后肠内(循环后期锥鞭毛体),长宽11.7~30.4µm×0.7~5.9µm。游离鞭毛自核的后方发出。在血液内,外形弯曲如新月状。
生活史
传播媒介为锥蝽,可栖息于人房内,多夜间吸血。主要虫种为骚扰锥蝽(Triatoma infestans)、长红锥蝽(Rhodnius prolixus)、大锥蝽(Panstrongylus megistus)、泥色锥蝽(T.sordida)等。
雌性或雄性锥蝽的成虫、幼虫、若虫都能吸血。当锥蝽自人体或哺乳动物吸入含有锥鞭毛体的血液,数小时后,锥鞭毛体在前肠内失去游离鞭毛,约在14~20小时后,转变为无鞭毛体,在细胞内以二分裂增殖。然后再转变为球鞭毛体(spheromastigote)进入中肠,发育为上鞭毛体。上鞭毛体以二分裂法增殖,约在吸血后第3、4天,上鞭毛体出现于直肠,并附着于上皮细胞上。第5天后,上鞭毛体变圆,发育为循环后期锥鞭毛体。当受感染的锥蝽吸血时,鞭毛体随锥蝽粪便经皮肤伤口或粘膜进入人体。
血液内的锥鞭毛体侵入组织细胞内转变为无鞭毛体,进行增殖,形成假囊(即充满无鞭毛的细胞),约5天后一部分无鞭毛体经上鞭毛体转变为锥鞭毛体,锥鞭毛体破假囊而出进入血液,再侵入新的组织细胞。
此外,还可通过输血、母乳、胎盘或食入被传染性锥蝽粪便污染的食物而获得感染。
致病
潜伏期为1~3周,此期无鞭毛体在细胞内繁殖,所产生的锥鞭毛体在细胞之间传播,并存在于血液中。
急性期 锥虫侵入部位的皮下结缔组织出现炎症反应,局部出现结节,称为夏氏肿(Chagoma)。如侵入部位在眼结膜则一侧性眼眶周围水肿、结膜炎及耳前淋巴结炎(Romana氏征)。这两种体征的病变都是以淋巴细胞浸润和肉芽肿为特点。主要临床表现为头痛、倦怠和发热、广泛的淋巴结肿大以及肝脾肿大。还可出现呕吐、腹泻或脑膜炎症状。心脏症状为心动过缓、心肌炎等。此期持续4~5周,大多数患者自急性期恢复,病程进入隐匿期,有些患者则转为慢性期。
慢性期 常感染后10~20年后出现,主要病变为心肌炎,食管与结肠的肥大和扩张,继之形成巨食管(megaesophagus)和巨结肠(megacolon)。病人进食和排便均感严重困难。在慢性期,血中及组织内很难找到锥虫。
诊断
在急性期,血中锥鞭毛体多数多,可以采用血涂片。
在隐匿期或慢性期,血中锥虫少,用免疫学诊断法,也可用动物接种诊断法,即用人工饲养的锥蝽幼虫吸受检者血,10~30天后检查该虫肠道内有无锥虫。
分子生物学的PCR及DNA探针技术,对于检测虫数极低的血标本,也有很高的检出率。
流行和防治
夏格氏病广泛分布于中美洲和南美洲,主要在居住条件差的农村流行,患者的80%是幼年感染。
枯氏锥虫在多种哺乳动物寄生,如狐、松鼠、食蚁兽、犰狳、犬、猫、家鼠等。在森林的野生动物之间通过锥蝽传播。从野生动物传播到家养动物,再传播到人,而后在人群中流行。
硝基呋喃(nitrofuran)类衍生物Beyer2502(商品名Lampit)对急性期有一定效果,能降低血中虫数,使临床症状减轻。
改善居住条件和房屋结构,不使锥蝽在室内孳生。滞留喷洒杀虫剂可杀灭室内锥蝽。